上海吉玛制药技术有限公司
18 年
手机商铺
- NaN
- 0
- 0
- 1
- 0
推荐产品
公司新闻/正文
Nature Communication丨暨南大学研究团队揭示了阻断周细胞中NKX2-3的转录活性可显著抑制肿瘤血行转移的机制
20 人阅读发布时间:2026-05-07 17:17
2025年08月02日,暨南大学药学院叶文才/张冬梅研究团队在《Nature Communication》(IF=15.7)上发表了题为” Pericytes promote metastasis by regulating tumor local vascular tone and hemodynamics”的研究论文。该研究揭示了TPCs调控的血管舒张和血流动力学调控促进肿瘤转移,为肿瘤转移提供了潜在的预后指标和治疗策略。值得注意的是,在本研究中,作者使用吉玛提供的siRNAs、miRNA mimics and inhibitors、腺相关病毒以研究TPCs对结直肠癌转移的影响。

远处转移是癌症死亡的主要原因,而血行转移是肿瘤远处转移的主要机制。血行转移主要包括肿瘤细胞侵入血管、循环肿瘤细胞(CTC)建立、肿瘤细胞外渗至其他器官和转移灶定植等阶段。其中,肿瘤细胞侵入血管是血行转移的早期阶段。现有的研究主要集中于肿瘤细胞、内皮细胞(EC)和巨噬细胞对肿瘤细胞侵入的影响。然而,肿瘤细胞侵入的机制尚不明确,仍然缺乏有效的治疗药物和策略。从新的角度探索肿瘤细胞侵入的机制,有助于发现新的治疗靶点。
本研究发现结直肠癌肝转移 (CRCLM) 患者原发肿瘤的血管直径和血流量显著增加。同源框转录因子 (TF) NKX2-3 在 CRCLM 患者的肿瘤周细胞(TPC)中高表达,并与癌症患者的血源性转移呈正相关。肿瘤来源的细胞外囊泡 (EV) 通过长链非编码 RNA (lncRNA) NEAT1 /miR-769-5p 通路诱导 NKX2-3 在 TPC 中的过表达。NKX2-3 通过 PDE1C/cAMP/PKA 依赖的信号轴阻碍钙通道的激活,从而抑制 TPC 收缩,从而诱导肿瘤局部血管舒张,增加血流和血管渗漏。条件性敲除Nkx2-3或通过肽特异性阻断TPC中NKX2-3的转录活性可恢复局部血管收缩和血流动力学,从而改善肿瘤细胞的血源性转移。
下面,我们一起来了解具体的研究内容:
研究成果
1. 原发肿瘤血流动力学改变与结直肠癌肝转移相关
为了探讨血流动力学改变与临床肿瘤转移的关系,采集了有无转移的CRC患者原发灶的血流多普勒超声图像,并用Open CV计算血流信号强度。结果显示,与无转移患者相比,肝转移的CRC患者血流明显增多。此外,血流信号强度在CRCLM患者中表现为中等。免疫荧光分析显示,CRCLM患者原发灶微血管直径、长度和表面积均明显增加,而微血管密度无明显差异。此外,CRCLM患者原发灶血管基底膜完整性降低,并伴有乏氧增强。采用Pearson相关性分析显示微血管直径与血流信号呈正相关,而非微血管密度与血流信号呈负相关(图 1h-j)。然而,血流信号与肿瘤乏氧之间无显著相关性。这些数据提示原发灶血流增多与CRCLM密切相关。然而,血流动力学改变对肿瘤转移的调控作用尚不清楚。
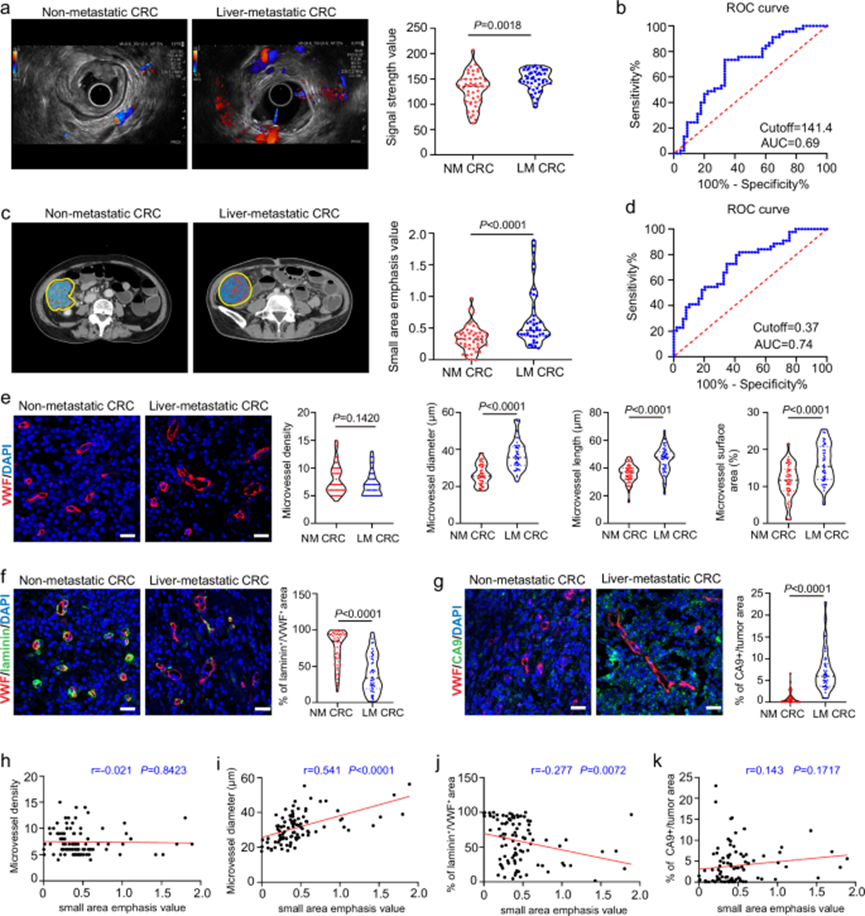
图1.原发肿瘤血流动力学改变与结直肠癌肝转移相关
2. NKX2-3在MAP中高表达并与结直肠癌肝转移相关
周细胞包裹在毛细血管周围,已知其可调节血管的收缩和血液灌注。因此,我们推测肿瘤周细胞是否可能参与调节肿瘤局部血管张力和血流动力学,从而导致肿瘤转移。我们之前的研究中通过 scRNA-seq 分析了来自有或无肝转移的 CRC 患者原发性肿瘤组织的 TPCs 。总体而言,TPCs 分为 13 个不同的簇,其中簇 3 的细胞丰度增加最显著,几乎只在 CRCLM 样本中被鉴定出来,因此被称为转移相关周细胞(MAPs)。GO 分析显示,MAPs 中富集的上调基因与免疫反应、细胞外基质组织和血管发育有关。为了进一步研究 TPCs 基因表达的潜在机制,确定了NKX2-3 在 MAPs 中排名最高 。接下来,比较了非转移性(TPC NM)和肝转移性(TPC LM )CRC 患者来源的 TPCs 中 NKX2-3 的表达。与TPC NM和肿瘤微环境中的其他细胞相比, TPC LM中NKX2-3的表达显著增加。而NKX2-3+阳性细胞比例达到44%时,能最有效区分结直肠癌肝转移病例,具有临床诊断应用价值(图 2h)。此外,NKX2-3 + TPCs 比例升高与 CRC 患者的总生存期 (OS)和无病生存期 (DFS)较差相关,提示TPCs中NKX2-3可能是肿瘤血行转移的危险因素,且与患者预后不良相关。
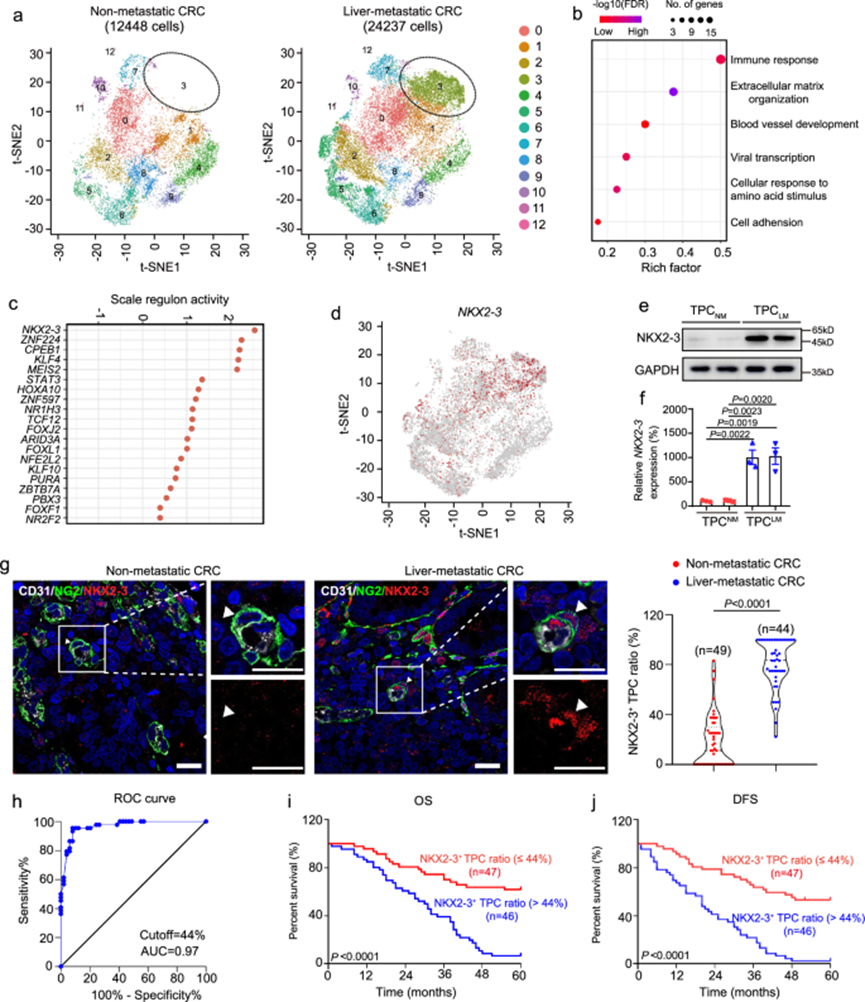
图2.NKX2-3在MAP中高表达并与结直肠癌肝转移相关
3. TPC 中的 NKX2-3 通过抑制 PDE1C/cAMP/PKA/Ca2+轴来抑制细胞收缩
鉴于NKX2-3高表达的TPCs与肿瘤转移相关,我们旨在研究NKX2-3在TPCs中的功能及其潜在机制。ChIP-seq结果显示TPCs中NKX2-3的峰值基因主要富集在钙信号通路。TPCs中NKX2-3过表达抑制了L型Ca2+激动剂(S)-(-)-Bay K8644刺激的钙内流。然后,对 TPCLMgNKX2-3与 TPCLMgNC进行 RNA-seq ,在 TPCLMgNKX2-3中发现 637 个下调基因。为了研究 TPCs 中 NKX2-3 调控钙信号传导的分子机制,通过维恩图分析钙信号通路相关的 NKX2-3 峰值基因与 TPCLMgNKX2-3中下调基因之间的重叠基因。在这两个列表之间发现了 5 个重叠基因,包括PDE1A、PDE1C、SLC8A1、CAMK2A和CAMK2D。在这些基因中, PDE1C和PDE1A的启动子可以与 NKX2-3 结合并受 NKX2-3 调控。有趣的是,只有TPCLM中PDE1C的敲低才会显着诱导 L 型钙电流。PDE1C 是一种磷酸二酯酶,可将 cAMP 水解为 AMP,随后抑制 PKA 诱导的钙转运。结果表明,TPCs 中 NKX2-3 的过表达会诱导 cAMP 的降解,而靶向 PDE1C 的 siRNA 可逆转这一过程并伴随钙转运增加。此外,用 TPC NM中的 H89·2HCl 抑制 PKA 活性NKX2-3+siPDE1C降低了钙电流。这些数据表明 TPCs 中的 NKX2-3 通过 PDE1C/cAMP/PKA 信号轴抑制钙电流。
细胞内钙振荡是血管周围细胞收缩的关键调节因子,它促进肌球蛋白轻链 (MLC) 的磷酸化并诱导血管收缩。事实上,结果表明,与 TPC NM组相比,NKX2-3 过表达抑制了 TPCs收缩,表现为形状从梭形转变为菱形、胶原收缩能力下降及 p-MLC2Ser15表达降低。正如预期的那样,与 TPCNMNKX2-3+siNC组相比,PDE1C 敲低促进了 TPC 收缩,而 PKA 活性或钙通道的药理抑制逆转了 TPCNMNKX2-3+siPDE1C的收缩。总之,这些数据表明 NKX2-3 通过 PDE1C/cAMP/PKA 依赖性信号轴阻碍 L 型钙通道的活性,从而抑制 TPC 收缩。
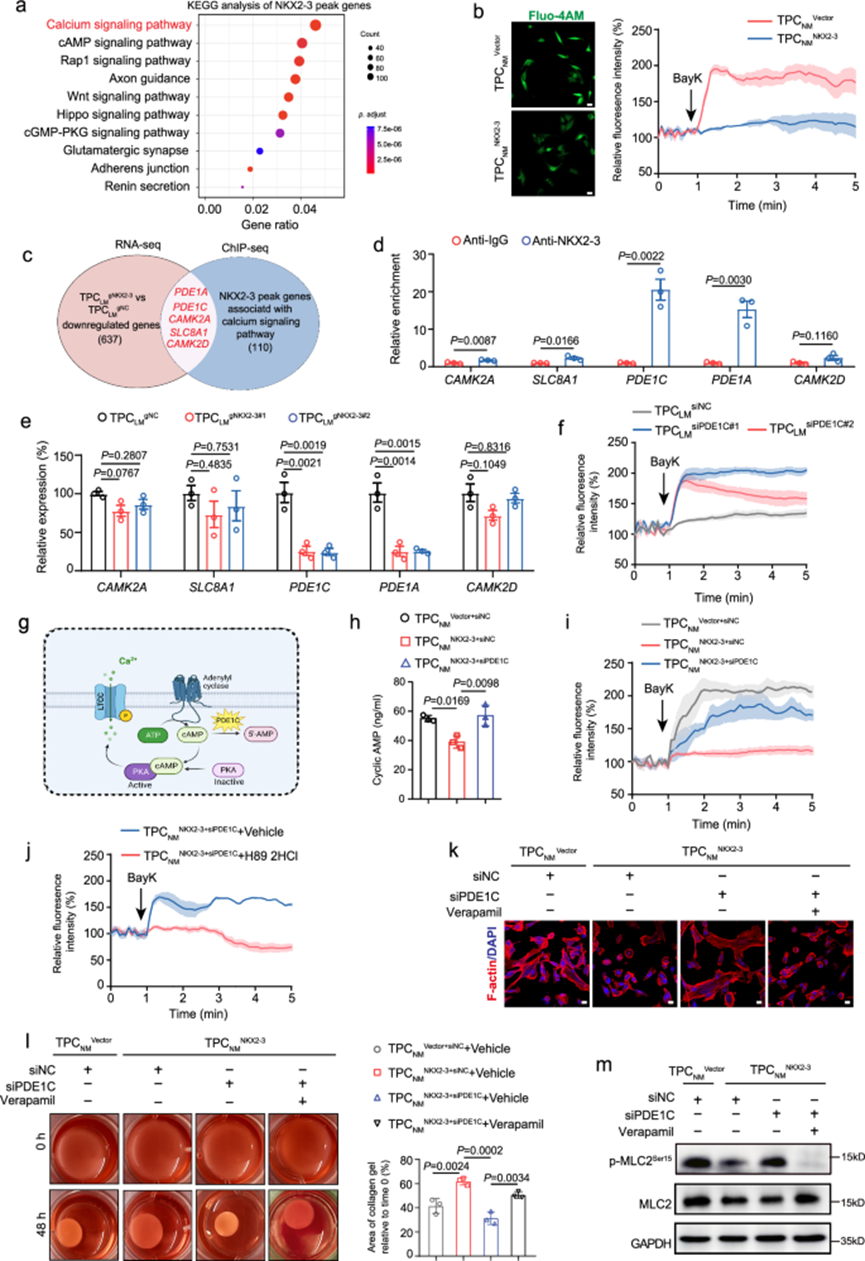
图3.NKX2-3通过抑制钙信号传导来调节TPC收缩
4. 周细胞特异性敲除Nkx2-3促进肿瘤局部血管收缩,抑制肿瘤转移
鉴于TPCs中的NKX2-3与肿瘤转移相关,进一步在体内研究周细胞NKX2-3对肿瘤转移的影响及其相关机制。将Cspg4 -CreERT小鼠与ROSA26-loxP-stop-loxP-tdTomato小鼠杂交得到目标小鼠(PClin小鼠),再将PClin小鼠与Nkx2-3flox/flox小鼠杂交得到周细胞-Nkx2-3特异性敲除小鼠(PClin-KO小鼠)。注射他莫昔芬后,TPCs被tdTomato荧光标记,PClin和PClin-KO小鼠的TPCs标记情况相似,此外,注射他莫昔芬后,PClin-KO小鼠的TPC中NKX2-3减少。 为了探究TPCs中NKX2-3对CRC转移的影响,将MC-38-luc-LM3细胞注射到PC lin和PC lin-KO小鼠的盲肠壁中,进行活体成像。 TPCs 中Nkx2-3的缺失对非肿瘤组织和肿瘤生长的影响微乎其微,而 CRCLM 受到显著抑制,这表现为肝转移灶减少和 CTC 减少。这些数据表明 TPC 中的 NKX2-3 促进肿瘤血行转移。
由于TPCs中的NKX2-3抑制细胞收缩,因此我们研究了TPCs中的NKX2-3是否通过调节血管张力来诱导肿瘤转移。应用光片和共聚焦荧光显微镜分析了血管形态和结构。条件性敲除Nkx2-3对周细胞覆盖率和血管密度的影响可以忽略不计。然而,PClin-KO小鼠原发性肿瘤的血管网络结构与PClin小鼠不同,其特点是平均血管直径与PClin小鼠相比显着减小,这可能是由于大直径血管比例减少。然后,用双光子显微镜检查小鼠原发性肿瘤中的血管收缩和血管舒张。U46619 是血栓素 A (2) 类似物,可作为毛细血管的血管收缩剂。我们的结果表明,U46619 治疗后,PClin-KO小鼠的毛细血管直径减少了约 20% ;然而,在 PClin小鼠中没有观察到明显变化 ,这表明 TPCs 中的 NKX2-3 诱导血管舒张。此外,TPCs 的细胞内钙水平由钙指示剂 GCaMP6 测定,而 GCaMP6 由 TPC 中的Cspg4启动子驱动。我们的结果表明,与PClin-GCaMP6小鼠相比, PClin-KO-GCaMP6小鼠细胞内Ca 2+对U46619的反应显著增加。总之,TPCs中的NKX2-3通过抑制钙通道活性来诱导血管舒张和肿瘤转移。
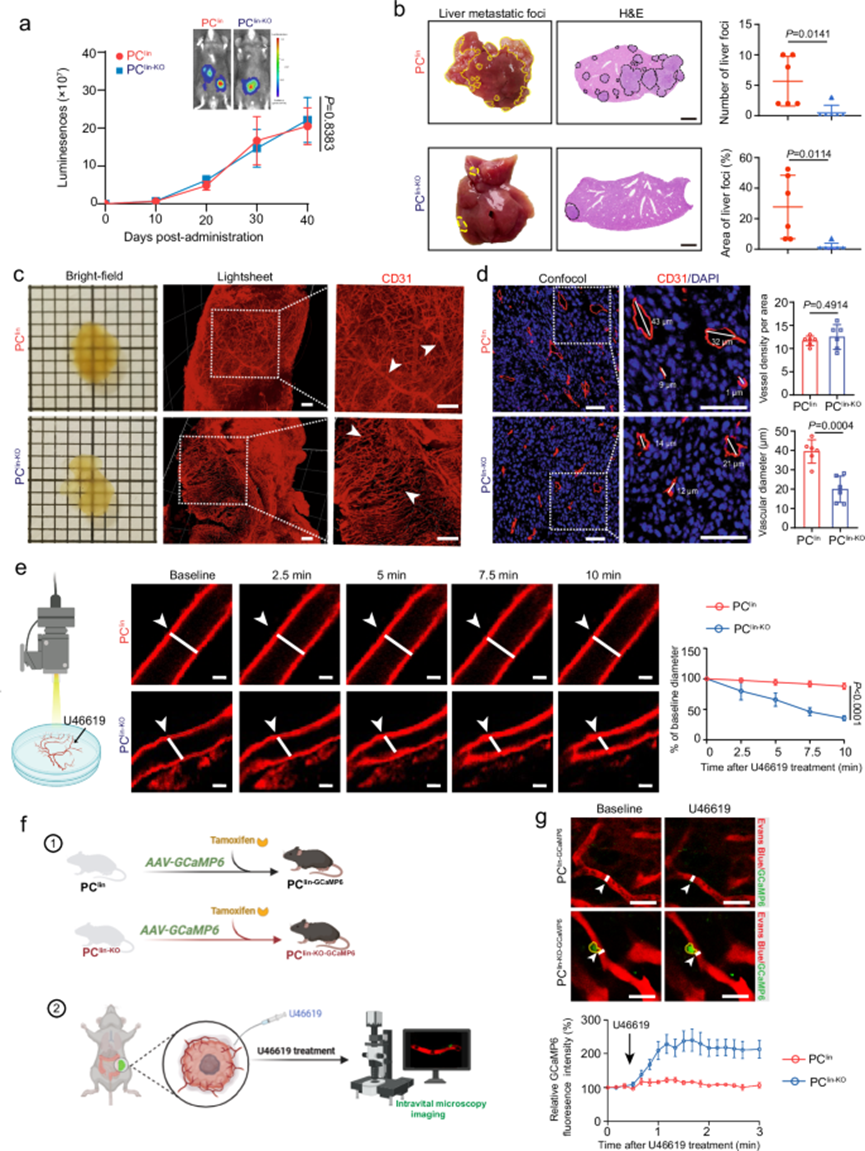
图4.周细胞特异性敲除Nkx2-3促进肿瘤局部血管收缩,抑制肿瘤转移
5. TPC 中的 NKX2-3 通过增加血流和血管通透性促进肿瘤转移
由于周细胞收缩和舒张可以通过血管收缩或扩张直接调节血流动力学,或通过打开内皮连接间接影响血管渗漏,研究者试图确定 TPCs 中的 NKX2-3 是否对原发性肿瘤的血流动力学和血管通透性产生影响。通过双光子成像评估血流速度,与PClin小鼠相比,PClin-KO小鼠的血流速度明显减弱。此外,对 PClin和 PClin-KO小鼠进行了 MRI 成像,我们的结果显示, TPC 中Nkx2-3的删除导致灌注减少。与 MRI 实验一致,激光散斑对比成像显示与 PClin小鼠相比,PClin-KO小鼠的微血管血流减弱 。TPCs 中Nkx2-3的删除增强了 EC 之间的紧密连接。此外,PClin-KO小鼠的血管通透性明显低于 PClin小鼠。为了进一步探究PClin小鼠中观察到的血管扩张是否有利于肿瘤细胞内渗, 我们构建了微流控血管芯片模型 。结果显示,与TPC NM相比,TPCNMNKX2-3显著促进了HCT116细胞穿过血管屏障。此外,体内实验表明,在用血管扩张剂治疗后,绿色荧光蛋白 (GFP) 标记的肿瘤细胞能够迅速穿过血管壁进入血液循环,这表明血管扩张有助于肿瘤细胞内渗和转移。综上所述,这些结果表明,TPC 中的 NKX2-3 是毛细血管血流和血流速度以及血管渗漏的关键调节器,从而为肿瘤细胞转移铺平了道路。
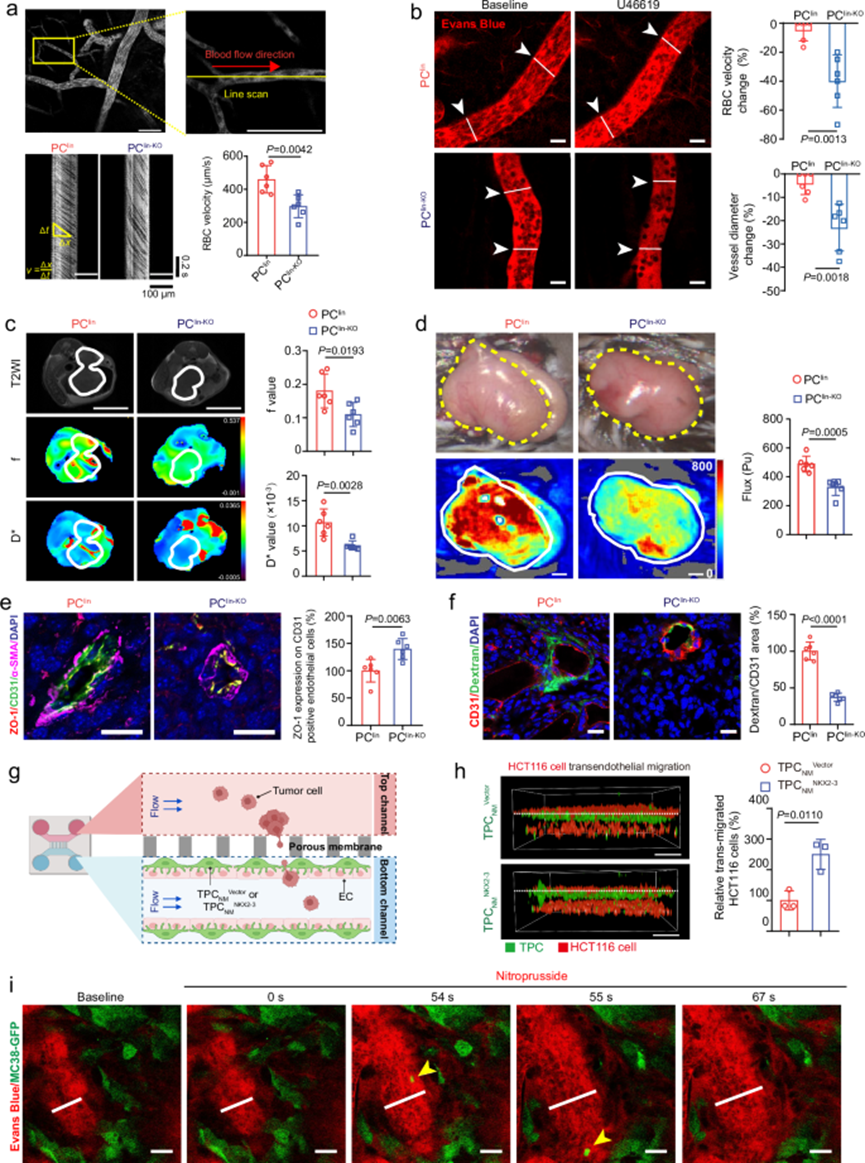
图5.TPC 中的 NKX2-3 通过增加血流和血管通透性促进肿瘤转移
6. 肿瘤衍生的 EV 通过 lncRNA NEAT1 /miR-769-5p 信号轴诱导 TPC 中 NKX2-3 的表达
越来越多的证据表明,EVs是肿瘤微环境中细胞间通讯的重要介质,而lncRNAs则被选择性地包装到EVs中并被受体细胞吸收。LncRNA NEAT1被发现是MAPs中高表达的lncRNA之一。NEAT1上调了NKX2-3转录与蛋白水平的表达。LncRNA可能作为竞争性内源性RNA(ceRNA)来吸收微小RNA(miRNA),从而抑制miRNA的功能并降低其对靶mRNA的调控作用。使用miRDB、miRTarBase、TargetScan和miRWalk数据库进行可能调控NEAT1的miRNA生信分析,并筛选出miR-769-5p。 LncRNA NEAT1可以与 miR-769-5p 结合并抑制 miR-769-5p 水平 。同样,miR-769-5p 模拟物与NKX2-3结合后可以上调NKX2-3 表达。这些结果表明MAPs中的NEAT1通过调控miR-769-5p的表达进而影响NKX2-3 表达。
为了进一步研究 MAPs 中NEAT1的高表达是否由来自肿瘤细胞的 EVs 引起的。从 DLD-1 细胞中纯化并鉴定了 EVs。从NEAT1过表达的 DLD-1 细胞释放的 EVs可被 TPCs 吸收,导致 miR-769-5p 降低,进一步引起NKX2-3 表达升高。此外,通过敲低 Rab27A 干扰 DLD-1 细胞中 EVs 的产生,可降低TPCs 中NEAT1和NKX2-3的表达,而 miR-769-5p 的水平升高。随后,与非转移性 CRC 患者相比,在人类 CRC 的原发性肿瘤和血液循环中检测到了NEAT1的水平。我们发现NEAT1在肿瘤细胞和 TPCs以及 CRCLM 患者的血液循环 EVs中高度富集。总之,这些数据表明 CRC 细胞衍生的NEAT1通过充当 miR-769-5p 的 ceRNA 诱导 TPCs 中的 NKX2-3 表达。
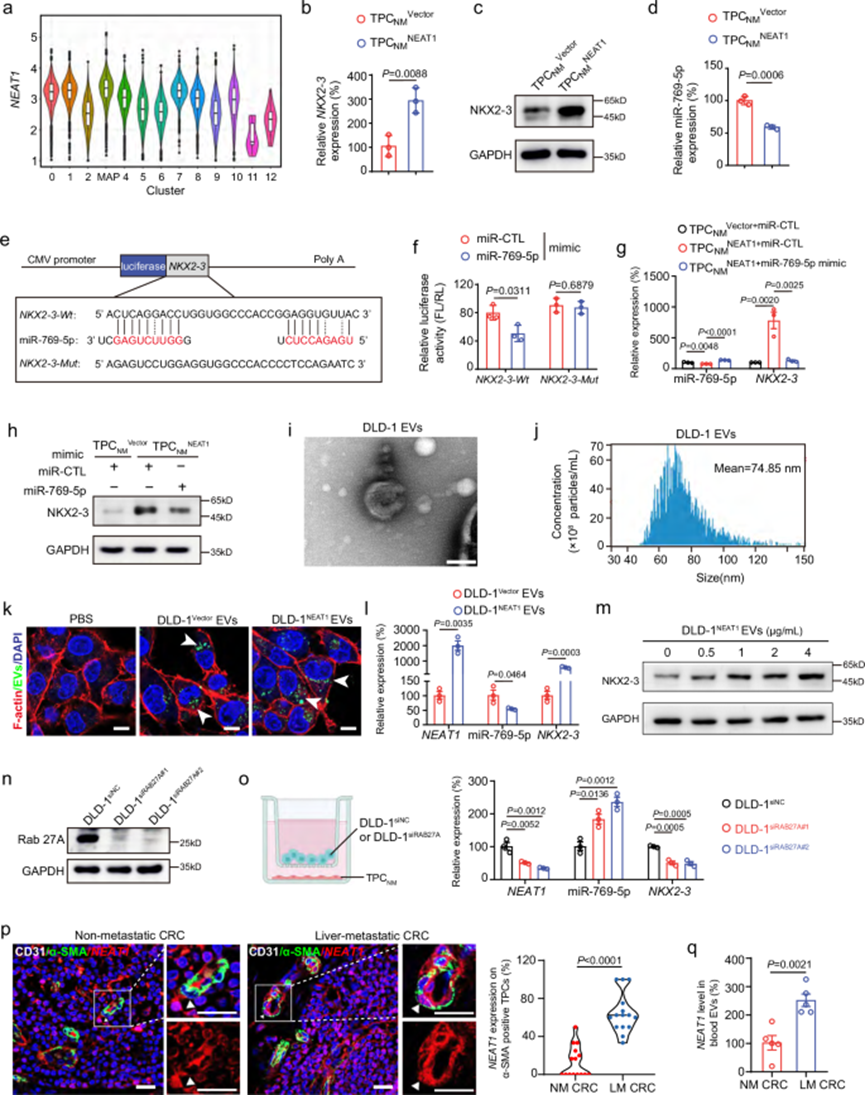
图6.肿瘤衍生的EV通过lncRNA NEAT1 / miR769-5p上调TPC中的NKX2-3表达
7. 靶向 NKX2-3高TPC 通过诱导血管收缩来抑制 CRCLM
接下来研究了阻断 NKX2-3 与PDE1C的结合是否可以抑制肿瘤转移。来自转录因子的寡肽可以竞争性地与其靶 DNA 序列结合,从而阻断 TF 与 DNA 的结合。因此,这可能是抑制 NKX2-3 与PDE1C结合的有效方法。首先,通过AlphaFoldDB数据库预测了NKX2-3的蛋白质结构,局部距离差异检验的p值分析显示,152-206位残基为高置信度结构域。根据生信结果,合成了六条寡肽(称为 NB1 至 NB6)。其中NB2与PDE1C的结合亲和力最高 ,并能进一步阻断NKX2-3与PDE1C启动子的结合,但NB2对NKX2-3表达的影响微乎其微,因此选择NB2作为候选寡肽。成纤维细胞活化蛋白α(FAPα)是一种II型整合膜丝氨酸蛋白酶。为了提高NB2在TPCs中的递送效率,我们通过将NB2与Z-GP偶联,合成了一种FAPα活化的前药Z-GP-NB2。
为了进一步研究了NB2和Z-GP-NB2在体内的作用。采用Z-GP-NB2研究其抗转移作用及机制。Z-GP-NB2抑制了TPCNMNKX2-3诱导的HCT116异种移植瘤肝转移。此外,与对照组相比,Z-GP-NB2 治疗引起血管收缩,并伴有血管直径减小、血流量降低和血流速度降低,但减轻了肿瘤缺氧并增加了肿瘤血管的完整性。总之,这些数据表明抑制 TPCs 中 NKX2-3 的转录活性可以改善血管功能并抑制肿瘤转移。
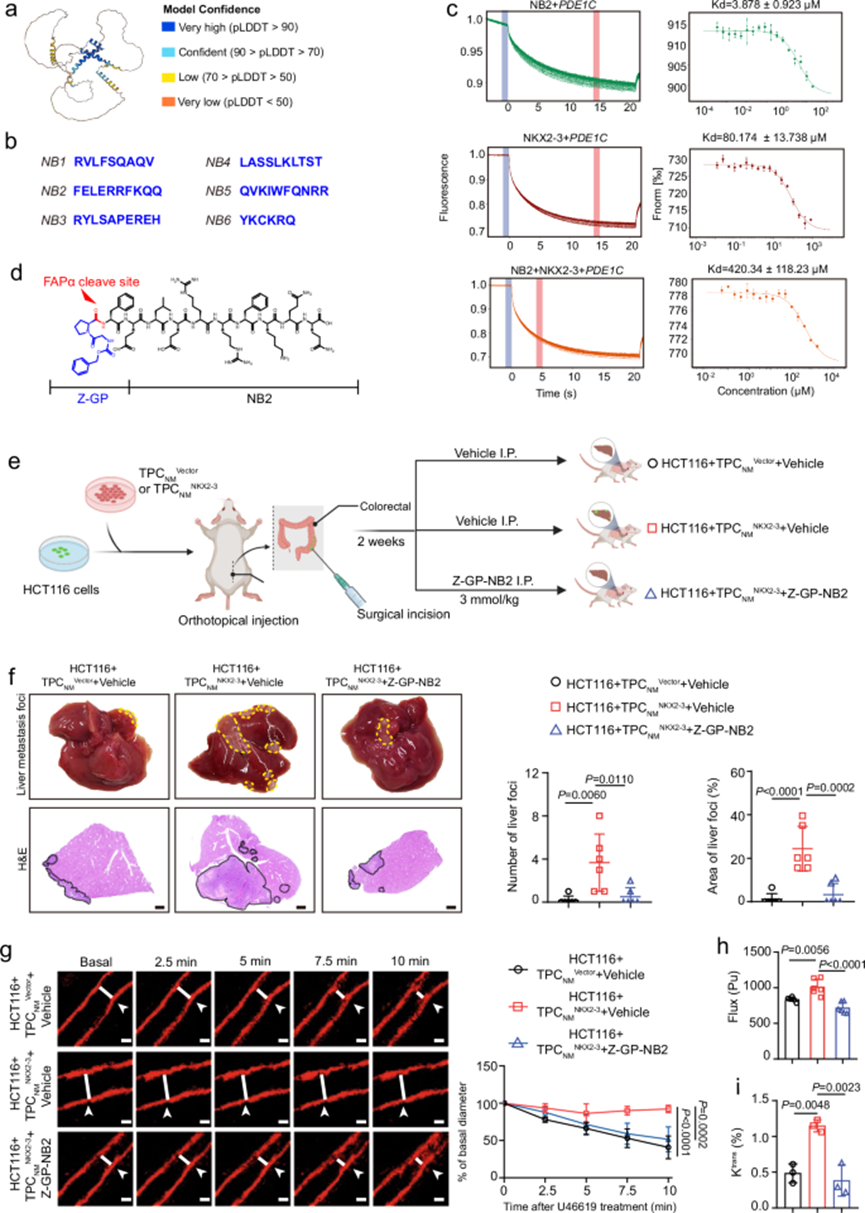
图7.阻断NKX2-3的转录活性可抑制肿瘤转移
综上所述,本研究发现NKX2-3高表达的TPCs通过诱导肿瘤组织局部血管扩张促进肿瘤细胞内渗,而阻断TPCs中NKX2-3的转录活性可显著抑制肿瘤血行转移。揭示TPCs在调节肿瘤血管张力、影响肿瘤细胞内渗及血行转移中发挥重要作用,为早期抑制肿瘤血行转移提供了潜在的预后指标和治疗靶点。
参考文献
Li, Xiaobo, et al. Pericytes promote metastasis by regulating tumor local vascular tone and hemodynamics. Nature Communications 16.1 (2025): 7115.


